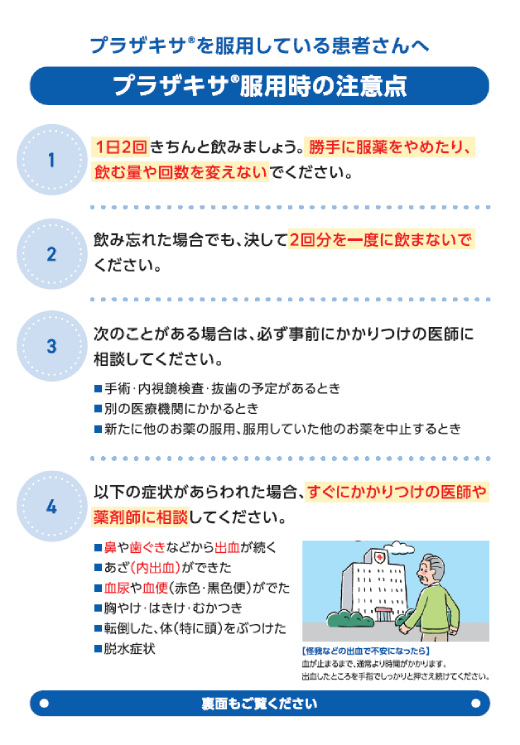
製剤写真・組成・性状
組成・性状
| 成分名 | ダビガトランエテキシラートメタンスルホン酸塩 |
|---|---|
| 領域名 | 循環器疾患 |
| 成分・含量 | 1カプセル中 ダビガトランエテキシラートメタンスルホン酸塩 86.48mg (ダビガトランエテキシ ラートとして75mg) |
| 剤形・色調 | 頭部及び胴部不透明な白色の硬カプセル剤 |
| 内容物 | 淡黄色の顆粒 |
| 外形 |

2号 |
| 識別コード |  |
| 長さ | 約18mm |
| 直径 | 約6mm |
| 重さ | 約0.28g |
剤形

包装形態
※アルミピローの画像の次にPTPシートの画像があります。


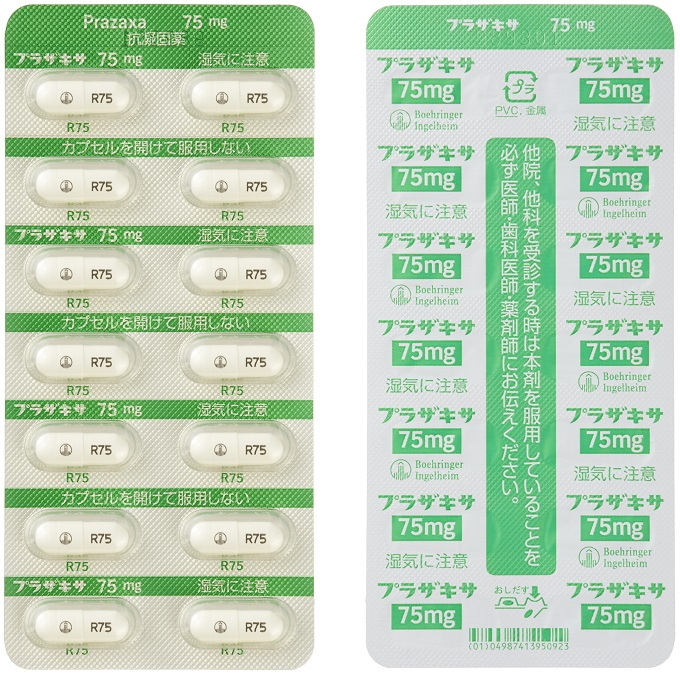
コード・番号表
| 日本標準商品分類番号 | 873339 |
|---|---|
| 承認番号 | 22300AMX00433000 |
| 薬価基準収載 医薬品コード |
3339001M1024 |
| レセプト電算処理コード | 622043301 |
包装:112カプセル
| JANコード | 4987413261616 |
|---|---|
| HOT7(処方用番号) | 1204339 |
| HOT番号 | 1204339010201 |
| 販売包装単位コード | (01)14987413261613 |
| 調剤包装単位コード | (01)04987413950923 |
よくある質問
-
アルミピロー包装開封後は、湿気を避けて保存し、できるだけ早くご使用下さい。
<引用>
プラザキサカプセル 電子添文 -
ビタミンK拮抗薬(ワルファリン)からプラザキサに変更する際は、PT-INR2.0未満の場合は当日にプラザキサの投与を開始し、PT-INR2.0以上の場合はPT-INR2.0未満が確認されたのちにプラザキサの投与を開始してください。
<引用>
プラザキサカプセル 電子添文
プラザキサ適正使用のポイント -
簡易懸濁法による投与はお勧めできません。
簡易懸濁法による溶解性、安定性、チューブへの吸着性は検討しておりません。
脱カプセル後の薬物動態データより、本剤は簡易懸濁法には適さないと判断されました。 -
本剤をカプセルから出して服用しないでください。
<参考>
本剤の内容物を25℃/75% R.H.で保存したとき、1日で規格外となる結果を得ました。内容物のみを服用した場合、カプセルでの服用に比べてダビガトランの血中濃度が上昇するおそれがあります。本剤の安定性・安全性を担保するため、カプセル剤を開けて服用しないよう指導して下さい。<引用>
プラザキサカプセル インタビューフォーム ⅩⅢ.備考 1.調剤・服薬支援に際して臨床判断を行うにあたっての参考情報 -
本剤は吸湿性があるため、本剤を一包化することは避けて頂くようにお願いします。
「本剤は吸湿性があるので、服用直前にPTPシートから取り出すよう指導すること。」(14. 適用上の注意、14.1.2 )<参考>
無包装状態での安定性(PTP包装開封後)
本剤の無包装品を40℃/75%R.H.で保存した時、2時間で規格外となる結果を得ました。また、本剤の無包装品を30℃/75%R.H.及び25℃/60%R.H.で保存したとき、6時間は規格内でしたが、12時間で規格外となる結果を得ました。本剤をPTP包装から取り出して処方しないようお願い致します。<引用>
プラザキサカプセル 電子添文
プラザキサカプセル インタビューフォーム Ⅳ.製剤に関する項目 6.製剤の各種条件下における安定性